2014年大綱版高考理綜真題試卷附答案
一、選擇題
1、下列有關細胞核的敘述,錯誤的是( )
A.蛋白質是細胞核中染色質的組成成分
B.細胞核中可進行遺傳物質的復制和轉錄
C.小分子物質可以通過核孔,大分子物質不能
D.有絲分裂過程中存在核膜消失和重新形成的現象
2.ATP是細胞中重要的高能磷酸化合物。下列有關ATP的敘述,錯誤的是( )
A.線粒體合成的ATP可在細胞核中發揮作用
B.機體在運動時消耗ATP,睡眠時則不消耗ATP
C.在有氧與缺氧的條件下細胞質基質中都能形成ATP
D.植物根細胞吸收礦質元素離子所需的ATP來源于細胞呼吸作用
3、下列關于人體淋巴細胞的敘述,錯誤的是( )
A.在胸腺中發育成熟的T淋巴細胞可參與細胞免疫
B.效應T淋巴細胞可攻擊被病原體感染的宿主細胞
C.T淋巴細胞和B淋巴細胞都是由造血干細胞發育成的
D.T細胞釋放的淋巴因子不能使受到抗原刺激的B細胞增殖
4.某同學在①、②、③三種條件下培養大腸桿菌,這三種條件是:
①以葡萄糖為碳源的培養基,不斷補充培養基,及時去除代謝產物
②以葡萄糖為碳源的培養基,不斷補充培養基,不去除代謝產物
③以葡萄糖和乳糖為碳源的培養基,不補充培養基,不去除代謝產物


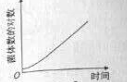
甲 乙 丙
A.甲、乙、丙 B.乙、丙、甲 C.丙、甲、乙 D. 丙、乙、甲
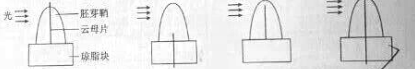
5.為驗證單側光照射會導致燕麥胚芽鞘中生長素分布不均勻這一結論,需要先利用瓊脂塊收集生長素,之后再測定其含量。假定在單側光照射下生長素的不均勻分布只與運輸有關。下列收集生長素的方法(如圖所示)中,正確的是( )
二、非選擇題

31.(9分)植物的光合作用受多種因素的影響。回答下列問題:
(1)右圖表示了 對某種C3植物和某種C4植物 的影響。當光照強度大于p時,C3植物和C4植物中光能利用率高的是 植物。通常提高光能利用率的措施有 的面積,補充 氣體等。
(2)在光合作用過程中,C4植物吸收的CO2被固定后首先形成 化合物。
(3)C3植物光合作用的暗反應需要光反應產生的ATP和NADPH,這兩種物質在葉綠體內形成的部位是 。NADPH的中文簡稱是 ,其在暗反應中作為 劑,用于糖類等有機物的形成。
32.(9分)小腸的吸收是指食物消化后的產物。水和無機鹽等通過小腸上皮細胞進入血液和淋巴的過程。0.9%的NaCl溶液是與兔的體液滲透壓相等的生理鹽水。某同學將處于麻醉狀態的兔的一段排空小腸結扎成甲、乙、丙、丁四個互不相同、長度相等的腸袋(血液循環正常),并進行實驗,實驗步驟和實驗結果如表:

請根據實驗結果回答問題:
(1)實驗開始時,水在腸腔和血液之間的移動方向是:甲組從 ;丙組從 。在這一過程中水分子的運動方向是從容液濃度 處流向溶液濃度
處。本實驗中水分子的這種移動過程稱為 。
(2)比較乙和丁的實驗結果,可推測小腸吸收Na+時,需要 的參與。
33.(10分)現有A、B兩個密閉、透明的生態瓶,其生物組成和光照條件見下表。一段時間后,發現A瓶的生態系統較B瓶穩定。
生態瓶編號 | 光照 | 含微生物的泥沙 | 浮游藻類 | 水草 | 浮游動物 |
A | + | + | + | + | + |
B | - | + | + | + | + |
注“+”表示有,“-”表示有。
請回答:
(1)A瓶中微生物、浮游藻類、水草和浮游動物共同組成了一個 ,浮游藻類和水草的種間關系為 。
(2)一段時間后,B瓶中浮游藻類種群密度 ,原因是 ;浮游動物的種群密度 ,原因是 。
(3)生態系統中分解者的作用是 。
34.(14分)現有4個小麥純合品種,即抗銹病無芒、抗銹病有芒、感銹病無芒、感銹病有芒,已知抗銹病對感銹病為顯性,無芒對有芒為顯性,且這兩對相對性狀各由一對等位基因控制。若用上述四個品種組成兩個雜交組合,使其F1均為抗銹病無芒,且這兩個雜交組合的F2表現型及其數量比完全一致。回答問題:
(1)為實現上述目的,理論上,必需滿足的條件有:在親本中控制這兩對相對性狀生物兩對等位基因必須位于 ,在形成配子時非等位基因要 ,在受精時雌雄配子要 ,而且每種合子(受精卵)的存活率也要 。那么。這兩個雜交組合分別是 和 。
(2)上述兩個雜交組合的全部F2植株自交得到F3種子,1個F2植株上所結的全部F3種子種在一起,長成的植株稱為1個株系。理論上,在所有F3株系中,只表現出一對性狀分離的株系有4種,那么,在這4種株系中,每種株系的表現型及其數量比分別是 , , 和 。
2014年普通高等學校招生全國統一考試(全國大綱卷)
理科綜合能力測試化學部分
第I卷
6.下列敘述正確的是
A.錐形瓶可用作加熱的反應器
B.室溫下,不能將濃硫酸盛放在鐵桶中
C.配制溶液定容時,俯視容量瓶刻度會使溶液濃度偏高
D.用蒸餾水潤濕的試紙測溶液的pH,一定會使結果偏低
7.NA表示阿伏加德羅常數,下列敘述正確的是
A. lmol FeI2與足量氯氣反應時轉移的電子數為2NA
B.2 L0.5 mol • L-1硫酸鉀溶液中陰離子所帶電荷數為NA
C.1 mol Na202固體中含離子總數為4NA
D.丙烯和環丙烷組成的42 g混合氣體中氫原子的個數為6 NA
8.下列敘述錯誤的是
A. SO2使溴水褪色與乙烯使KMnO4溶液褪色的原理相同
B.制備乙酸乙酯時可用熱的NaOH溶液收集產物以除去其中的乙酸
C.用飽和食鹽水替代水跟電石反應,可以減緩乙炔的產生速率
D.用AgNO3溶液可以鑒別KC1和KI
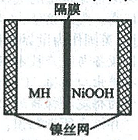
9.右圖是在航天用高壓氫鎳電池基礎上發展起來的一種金屬氫化物鎳電池(MH-Ni電池)。下列有關說法不正確的是
A.放電時正極反應為:NiOOH+H2O+e-→Ni(OH)2+OH-
B.電池的電解液可為KOH溶液
C.充電時負極反應為:MH+OH-→+H2O+M+e-
D.MH是一類儲氫材料,其氫密度越大,電池的能量密度越高
10.下列除雜方案錯誤的是
選項 | 被提純的物質 | 雜質 | 除雜試劑 | 除雜方法 |
A. | CO(g) | CO2(g) | NaOH 溶液、濃 H2SO4 | 洗氣 |
B. | NH4Cl(aq) | Fe3+(aq) | NaOH溶液 | 過濾 |
C. | Cl2(g) | HCl(g) | 飽和食鹽水、濃H2SO4 | 洗氣 |
D. | Na2CO3(s) | NaHCO3(s) | — | 灼燒 |
11.下列離子方程式錯誤的是
A.向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++ SO42 - =BaS04↓+2H2O
B.酸性介質中KMnO4氧化 H2O2:2MnO4- +5H2O2+6H+ = 2Mn2++5O2↑+ 8H2O
C.等物質的量的MgCl2、Ba(OH)2 和 HC1 溶液混合:Mg2++2OH-= Mg(OH)2↓
D.鉛酸蓄電池充電時的正極反應:PbSO4 + 2H2O-2e- = PbO2+4H++SO42 -
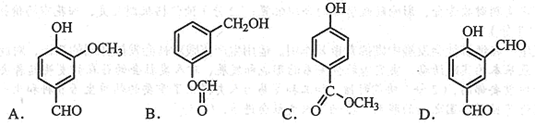
12.從香莢豆中提取的一種芳香化合物,其分子式為C8H8O3,遇FeCl3溶液會呈現特征顏色,能發生銀鏡反應。該反應可能的結構簡式是
13.已知:將Cl2通人適量KOH溶液,產物中可能有KC1、KClO、KC1O3,且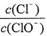 的值與溫度高低有關。當n(KOH)=amol時,下列有關說法錯誤的是A.若某溫度下,反應后
的值與溫度高低有關。當n(KOH)=amol時,下列有關說法錯誤的是A.若某溫度下,反應后 =11,則溶液中
=11,則溶液中 =2
=2
參加反應的氯氣的物質的量等于2amol
C.改變溫度,反應中轉移電子的物質的量ne的范圍:2amol≤ne≤6amol
D.改變溫度,產物中KC1O3的最大理論產量為7amol
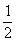 amol第II卷
amol第II卷
27.(15分)
A、B、D、E、F為短周期元素,非金屬元素A最外層電子數與其周期數相同,B的最外層電子數是其所在周期數的2倍。B 在D中充分燃燒能生成其最高價化合物BD2。E+與D2-具有相同的電子數。A在F中燃燒,產物溶于水得到一種強酸。回答下列問題:
(1)A在周期表中的位置是 ,寫出一種工業制備單質F的離子方程式 。
(2)B、D、E組成的一種鹽中,E的質量分數為43%,其俗名為 ,其水溶液與F單質反應的化學方程式為 ;在產物中加入少量KI,反應后加人CC14并振蕩,有 機層顯 色。
(3)由這些元素組成的物質,其組成和結構信息如下表:
物質 | 組成和結構信息 |
a | 含有A的二元離子化合物 |
b | 含有非極性共價鍵的二元離子化合物,且原子數之比為1:1 |
c | 化學組成為BDF2 |
d | 只存在一種類型作用力且可導電的單質晶體 |
a的化學式為 ;b的化學式為 ;;c的電子式為 ;
d的晶體類型是 。
(4)由A和B、D元素組成的兩種二元化合物形成一類新能源物質。一種化合物分子通過 鍵構成具有空腔的固體;另一種化合物(沼氣的主要成分)分子進入該空腔,其分子的空間結構為 。
)
28.(15分)
化合物AX3和單質X2在一定條件下反應可生成化合物AX5。回答下列問題:
(1)已知AX3的熔點和沸點分別為-93.6 ℃和76 ℃,AX5的熔點為167 ℃。室溫時AX3與氣體X2反應生成lmol AX5,放出熱量123.8 kJ。該反應的熱化學方程式為 。
(2)反應AX3(g)+X2(g) AX5(g)在容積為10 L的密閉容器中進行。起始時AX3和X2均為0.2 mol。反應在不同條件下進行,反應體系總壓強隨時間的變化如圖所示。
AX5(g)在容積為10 L的密閉容器中進行。起始時AX3和X2均為0.2 mol。反應在不同條件下進行,反應體系總壓強隨時間的變化如圖所示。

①列式計算實驗a從反應開始至達到平衡時的反應速率 v(AX5)= 。
②圖中3組實驗從反應開始至達到平衡時的反應速率v(AX5)由大到小的次序為 (填實驗序號);與實驗a相比,其他兩組改變的實驗條件及判斷依據是:b 、
c 。
③用p0表示開始時總壓強,p表示平衡時總壓強,α表示AX3的平衡轉化率,則α的表達式為
;實驗a和c的平衡轉化率:αa為 、αc為 。
29.(15 分)
苯乙酸銅是合成優良催化劑、傳感材料——納米氧化銅的重要前驅體之一。下面是它的一種實驗室合成路線:
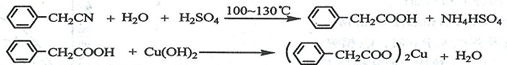
制備苯乙酸的裝置示意圖如下(加熱和夾持裝置等略):
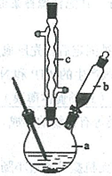
已知:苯乙酸的熔點為76.5 ℃,微溶于冷水,溶于乙醇。
回答下列問題:
(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸時,加入蒸餾水與濃硫酸的先后順序是
。
(2)將a中的溶液加熱至100 ℃,緩緩滴加40 g苯乙腈到硫酸溶液中,然后升溫至130 ℃繼續反應。在裝置中,儀器b的作用是 ;儀器c的名稱是 ,其作用是 。
反應結束后加適量冷水,再分離出苯乙酸粗品。加人冷水的目的是 。下列儀器中可用于分離苯乙酸粗品的是 (填標號)。
A.分液漏斗 B.漏斗 C.燒杯 D.直形冷凝管 E.玻璃棒
(3)提純粗苯乙酸的方法是 ,最終得到44 g純品,則苯乙酸的產率是 。
(4)用CuCl2 • 2H2O和NaOH溶液制備適量Cu(OH)2沉淀,并多次用蒸餾水洗滌沉淀,判斷沉淀洗干凈的實驗操作和現象是 。
(5)將苯乙酸加人到乙醇與水的混合溶劑中,充分溶解后,加入Cu(OH)2攪拌30min,過濾,濾液靜置一段時間,析出苯乙酸銅晶體,混合溶劑中乙醇的作用是 。
30.(15 分)
“心得安”是治療心臟病的藥物,下面是它的一種合成路線(具體反應條件和部分試劑略):
回答下列問題:
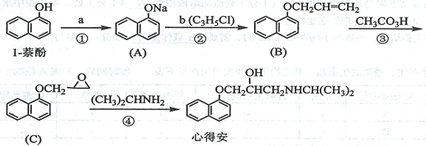
(1)試劑a是 ,試劑b的結構簡式為 ,b中官能團的名稱是 。
(2)③的反應類型是 。
(3)心得安的分子式為 。
(4)試劑b可由丙烷經三步反應合成:

反應1的試劑與條件為 ,
反應2的化學方程式為 ,
反應3的反應類型是 。(其他合理答案也給分)
(5)芳香化合物D是1-萘酚的同分異構體,其分子中有兩個官能團,能發生銀鏡反應,D能被KMnO4酸性溶液氧化成E( C2H4O2) 和芳香化合物F (C8H6O4),E和F與碳酸氫鈉溶液反應均能放出CO2氣體,F芳環上的一硝化產物只有一種。D的結構簡式為 ;
由F生成一硝化產物的化學方程式為 ,
該產物的名稱是 。
2014年全國全國統一招生考試大綱卷物理部分
二、選擇題:本題共8小題,每小題6分。在每小題給出的四個選項中,有的只有一項符合題目要求,有的有多項符合題目要求。全部選對的得6分,選對但不全的得3分,有選錯的得0分。
14.—質點沿x軸做直線運動,其I/-?圖像如圖所示。質點在/ = 0時位于x = 5m處,開始沿x軸正向運動。當k 8s.時,質點在軸上的位置為
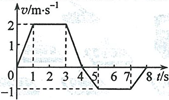
A. x = 3m B. x= 8m
C. a: = 9m D. x- 14m
15.地球表面附近某區域存在大小為150N/C、方向豎直向下的電場。一質量為1.00xl0_4kg、帶電量為-1.00x10—7C的小球從靜止釋放,在電場區域內下落10.0m。對此過程,該小球的電勢能和動能的改變量分別為(重力加速度大小取9.80m/s2,忽略空氣阻力)
A. -1.50x10_4J 和 9.95x10_3J B. 1.50 x 10_4J 和 9.95 x 10_3J
C. — 1.50x10_4J 和 9.65x10-3J D. 1.50 x 10_4J 和 9.65 x 10_3J
16.對于一定量的稀薄氣體,下列說法正確的是
A.壓強變大時,分子熱運動必然變得劇烈 B.保持壓強不變時,分子熱運動可能變得劇烈
C.壓強變大時,分子間的平均距離必然變小 D.壓強變小時,分子間的平均距離可能變小
17.在雙縫干涉實驗中,一鈉燈發出的波長為589nm的光,在距雙縫1.00m的屏上形成干涉圖樣。圖樣上相鄰兩明紋中心間距為0.350cm,則雙縫的間距為
A. 2.06x 10"7m B. 2.06x 10"4m C. 1.68x 10'4m '
18.兩列振動方向相同、振幅分別為扃和決的相干簡諧橫波相遇。下列說法正確的是
A.波峰與波谷相遇處質點的振幅為⑷-先|
B.波峰與波峰相遇處質點離開平衡位置的位移始終為肩+ A2
C.波峰與波谷相遇處質點的位移總是小于波峰與波峰相遇處質點的位移
D.波峰與波峰相遇處質點的振幅一定大于波峰與波谷相遇處質點的振幅
19.一物塊沿傾角為<9的斜坡向上滑動。當物塊的初速度為〃時,上升的最大高度為//,如圖所示;當物塊的初速度為|時,上升的最大高度記為A。重力加速度大小為g。物塊與斜坡間的動摩擦因數和h分別為

A. tan 0和與 B. tan 0和與2 {2gH ) 2
20.很多相同的絕緣銅圓環沿豎直方向疊放,形成一很長的豎直圓筒。一條形磁鐵沿圓筒的中心軸豎直放置,其下端與圓筒上端開口平 齊。讓條形磁鐵從靜止開始下落。條形磁鐵在圓筒中的運動速率 A.均勻增大 B.先增大,后減小 C.逐漸增大,趨于不變 D.先增大,再減小,最后不變
答:C
21.—中子與一質量數為A (A>1)的原子核發生彈性正碰。若碰前原子核靜止,則碰撞前與碰撞后中子的速率之比為 答:A
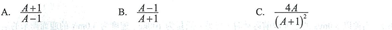

三、非選擇題:第22〜34題,共174分。按題目要求作答。
22.(6 分)
現用頻閃照相方法來研究物塊的變速運動。在一小物塊沿斜面向下運動的過程中,用頻閃相機拍攝的不同時刻物塊的位置如圖所示。拍攝時頻閃頻率是10Hz;通過斜面上固定的刻度尺讀取的5個連續影像間的距離依次為&、x2、x3、x4。已知@面頂端的高度/z和斜面的長度〜數據如下表所示。重力加速度大小g = 9.80m/s2。

根據表中數據,完成下列填空:
物塊的加速度a= m/s2(保留3位有效數字)。
⑵因為 可知斜面是粗糙的。
23.(12分)現要測量某電源的電動勢和內阻。可利用的器材有:電流表®,內阻為1.000; 電壓表®;阻值未知的定值電阻凡、.及2、及3、及4、尺5;開關S;—端連有鱷魚夾P的 導線1,其他導線若干。某同學設計的測量電路如圖U)所示。
(1)按圖(a)在實物圖(b)中畫出連線,并標出導線1和其P端。
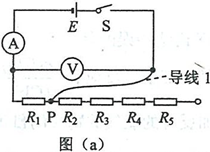
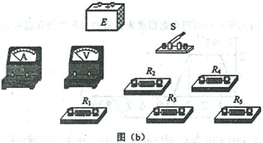
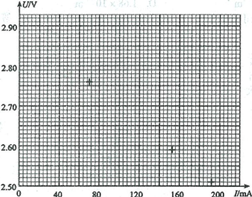
(2)測量時,改變鱷魚夾P所夾的位置,使及、R2、R3、及4、辦依次串入電路,記錄對應的電壓表的示數t/和電流表的示數/。 數據如下表所示。根據表中數據,在圖(c)中的坐標紙上將所缺數據點補充完整,并畫出C/-/圖線。

24.(12 分)
冰球運動員甲的質量為80.0kg。當他以5.0m/s的速度向前運動時,與另一質畺為100kg、速度為3.0m/s的迎面而來的運動員 乙相撞。碰后甲恰好靜止。假設碰撞時間極短,求:
(1 )碰后乙的速度的大小;
(2)碰撞中總機械能的損失。
25.(20 分)如圖,在第一象限存在勻強磁場,磁感應強度方向垂直于紙面(吁平面)向外;在第四象限存在勻強電場,方向沿x軸負向。在;;軸正半軸上某點以與X軸正向平行、大小為w的速度發射出一帶正電荷的粒子,該粒子在(d,0)點沿垂直于x軸的方向進人電場。不計重力。若該粒子離開電場時速度方向與軸負方向的夾角為<9,求<>
(1 )電場強度大小與磁感應強度大小的比值;
(2)該粒子在電場中運動的時間。